Obesidad
|
Fisiopatológica de la obesidad:
Control genético y epigenético La obesidad es una enfermedad multifactorial en cuyo origen inciden en forma recíproca una serie de genes neurorreguladores, termogénicos y controladores de absorción de alimentos, en conjunto con factores ambientales. Existe cierto consenso en considerar de forma independiente aquellos tipos de obesidad que tienen un origen exclusivamente genético y que se asocian a problemas de desarrollo físico e intelectual, ya que la causa está establecida, sea por alteraciones múltiples dominantes (síndrome de Prader Willi), autosómicas recesivas (síndrome de Bardet-Biedl) o ligadas al cromosoma X (síndrome de Wilson-Turner). También existe acuerdo en considerar de un modo particular la obesidad derivada de causas endocrinológicas conocidas, como ocurre en algunos casos de hipogonadismo o hipercortisolismo (síndrome de Cushing). Sin embargo, en la mayor parte de pacientes que desarrollan obesidad es difícil establecer una causa única, debido a la interacción con el ambiente y la modificación de la actividad de los genes candidatos. Estas variaciones en la expresión de los genes desencadenadas por el ambiente se ha denominado epigenética. La epigenética es una rama de la biología molecular que estudia los parámetros mediante los que un gen influido por el ambiente puede “expresarse” de forma diferencial y así aumentar o disminuir la producción de una proteína cuya función puede alterar vías específicas en la función de las células y producir enfermedad. Las alteraciones epigenéticas, a diferencia de las genéticas, no incluyen una alteración en la estructura del ADN (ácido desoxirribonucleico); es decir, la secuencia de nucleótidos se mantiene. Se presenta una alteración enzimática, por ejemplo, acetilación, metilación, deacetilación, demetilación o fosforilación de las histonas, proteínas a las que el ADN está estrechamente ligado en el cromosoma. Esta variación enzimática permite que la unión entre la secuencia de ADN y las proteínas histonas sea más o menos estrecha; lo que influye directamente sobre la capacidad de los genes de poder transcribir la información y expresar una función específica. Neurorregulación: Los sistemas que sostienen la regulación de la función en el intestino, el sistema nervioso central y las células adiposas actúan en forma integral. Por ejemplo, la inhibición de la digestión puede afectar las señales que regulan el centro de la saciedad, mientras cambios en el almacenamiento de la energía producen un fuerte efecto sobre los sistemas reguladores del apetito en el hipotálamo. De esta forma, el control del peso desde el punto de vista genético y funcional puede cambiar el comportamiento alimentario por diversas vías. El desequilibrio del balance energético que conduce a la obesidad es, pues, debido a una falta de control en la ingestión o en el gasto energético, a fallos en la regulación de las reservas lipídicas o a desajustes en la distribución de nutrientes entre los tejidos. Un aspecto importante que no es valorado en forma rutinaria y cuyos factores no son del todo conocidos, es el aspecto psicológico del control de la voluntad de ingerir alimentos y que finalmente determina el acto de comer. La respuesta individual a estímulos exteriores que influyen sobre un complejo de procesos neuronales dentro del cerebro y que en forma episódica estimulan, sostienen, terminan o incluso inhiben el deseo de alimentarse se relaciona con los factores internos que son determinados por la carga genética de cada individuo y que podríamos mencionar como tónicos cuya regulación es establecida por las reservas energéticas de la persona. El balance entre los aspectos episódicos y los aspectos tónicos que integran la influencia ambiental, los impulsos hedónicos de 22 experiencias previas, junto con las necesidades biológicas del cuerpo, determinan finalmente el comportamiento alimentario. |
Uno de la neurotransmisores más estudiados en el sistema
nervioso central es la serotonina (5-HT), cuyo mayor
papel está en la reducción de los deseos bulímicos de
alimentarse. Algunos circuitos que incluyen receptores
canabinoides y receptores de opioides tienen un papel
fundamental en la regulación de los eventos episódicos
de los deseos de alimentarse, particularmente en los tipos
de alimentos con alto contenido graso y densos en energía.
Todos estos neurotransmisores y péptidos juegan un
papel fundamental en la regulación de la alimentación y
son blancos farmacológico.
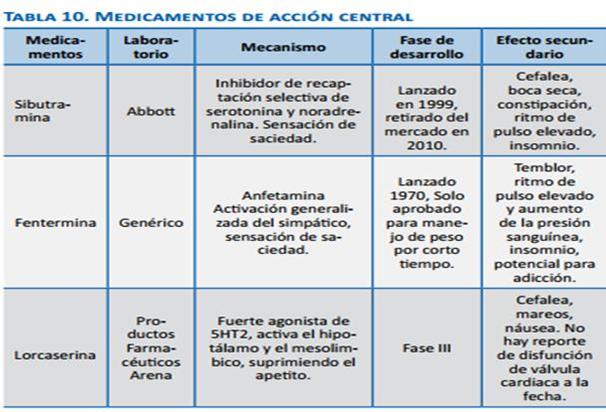
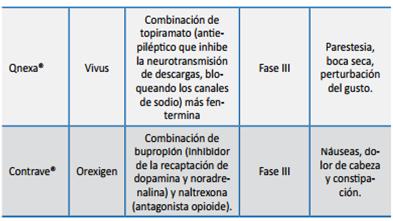
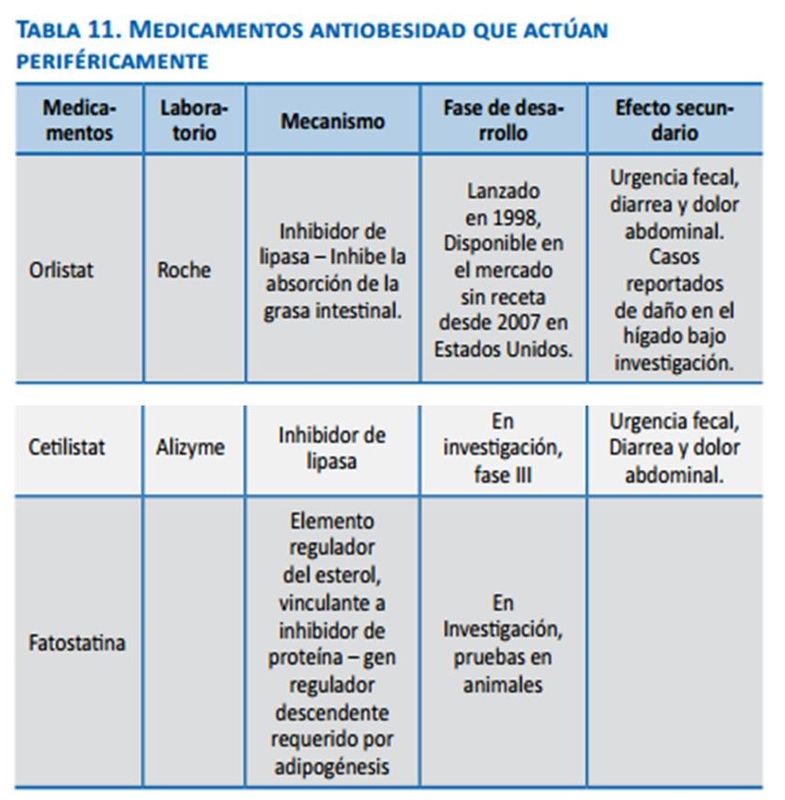
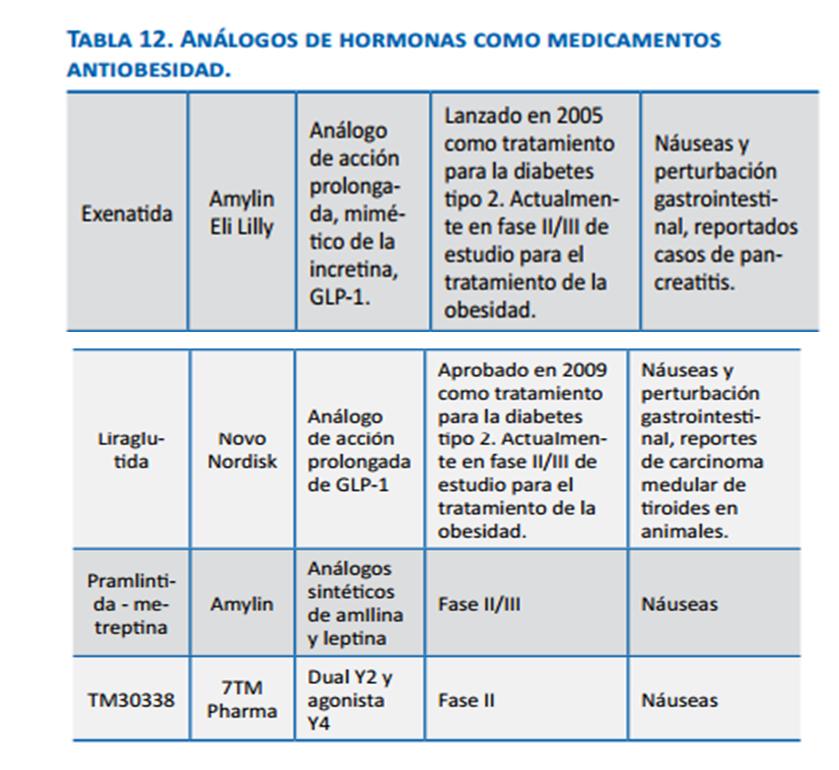
Dentro de los reportes de moléculas que pueden modular el gasto energético vía activación de UCP1 se halla la proteína del retinoblastoma (pRb). La supresión de la expresión de este gen en células fibroblásticas embrionarias de ratón conduce a la activación de genes de grasa parda, 25 incluso en condiciones en las que los ratones son sometidos a dieta rica en calorías, lo cual los hace resistentes a la obesidad. El pRb no se expresa en células precursoras de adipocitos marrón y, en pre-adipocitos blancos se une a los promotores de PGC1g (peroxisome proliferator activated receptor g activator 1), cuya función es generar biogenesis mitocondrial en las células marrones para aumentar la eficiencia del gasto calórico. La fisiología de la obesidad no puede ser desligada de las alteraciones en la regulación de los genes candidatos que pueden alterar el comportamiento alimentario, el gasto calórico y la adipogénesis. El reconocimiento de la forma como se integran estos factores es fundamental para la posibilidad de establecer un plan terapéutico. Tratamiento farmacológico de la obesidad: El manejo farmacológico de la obesidad actuaría básicamente a través de uno o más de los siguientes mecanismos: Efecto central (tabla 10): 1. Ya probadas en el mercado: anfetaminas, sibutramina, bloqueadores de los receptores canabinoides. Este tipo de medicamentos no existe en Colombia. En Estados Unidos existen: fentermina, dietilpropión y fendimetrazina. Estos medicamentos han sido asociados con HTA, hipertensión pulmonar, abuso y adicción, pues son estimulantes adrenérgicos que actúan centralmente, suprimiendo el apetito y aumentando el gasto energético a través de activación simpática generalizada, por eso la FDA no los ha aprobado para uso crónico en obesos y/o sobrepeso con IMC de 27 kg/m2 o más, con comorbilidades. Se recomienda no prolongar su consumo por más de tres meses. 2. En investigación: Qnexa®, Contrave® y Lorcaserina: todos en fase III. a. Qnexa®: combinación de fentermina y topiramato: el mecanismo exacto por el que disminuye el apetito no se conoce, pero es dosis dependiente. Los efectos colaterales más frecuentes son: parestesias, boca seca y disgeusia. Hace pocos días la FDA ordenó mayor seguimiento antes de salir al mercado 44 para descartar que aumentara el riesgo cardiovascular. b. Contrave®: combinación de bupropión, inhibidor de la recaptación de noradrenalina y serotonina, más naltrexona: antagonista opiáceo. Aumenta la actividad orexigénica en las neuronas hipotalámicas, mediante bloqueo sinérgico de las b-endorfinas, cada uno por separado disminuye el apetito. c. Agonistas 5 –HT2c: lorcaserina es un agonista selectivo de los receptores de serotonina 5-HT2c, y no actúa en los 5-HT2b (donde actúa la fenfluramina en las válvulas cardiacas), suprimiendo el apetito a nivel central en sitios que tienen que ver con recompensa y estado de ánimo, así también en otras áreas que regulan el apetito: hipotálamo y núcleos del tracto superior (NTS) |
|