Insuficiencia suprarrenal en urgencias
|
Insuficiencia suprarrenal en urgencias y en cuidado crítico:
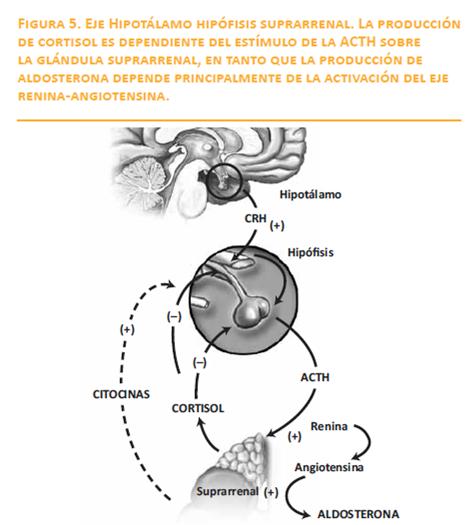
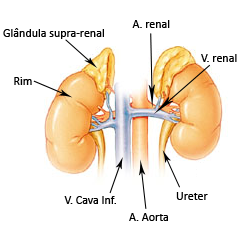
La corteza de la glándula suprarrenal humana sintetiza y secreta tres grandes tipos de hormonas esteroideas: los glucocorticoides, de los cuales el más importante es el cortisol, los mineralocorticoides (aldosterona) y algunos esteroides sexuales como dehidroepiandrosterona (DHEA) y dehidroepiandrosterona sulfato (DHEAs). Las respuestas adaptativas ante el estrés producido por el dolor o la enfermedad aguda, la hipotensión, la hipovolemia o el ayuno son provistas en buena medida por el cortisol y la aldosterona. Durante el estrés originado por el ayuno, el cortisol estimula la glucogenólisis y promueve la ruptura de proteínas en el músculo, con la consecuente liberación de aminoácidos, brindando el sustrato necesario para la gluconeogénesis en el hígado y en el músculo. Así mismo, el cortisol favorece la lipólisis suscitando liberación de ácidos grasos libres y glicerol, efectos que también pueden registrarse en circunstancias como el choque séptico y otros estados inflamatorios sistémicos, en los cuales la producción de hormona adrenocorticotrópica (ACTH) puede verse incrementada al parecer por mediación de interleucina 1 (IL-1). La aldosterona, por su parte, particularmente a través del efecto de retención renal de sodio, contribuye a la homeostasis del agua y a la adaptación frente a los estados de hipovolemia o hipoperfusión. El cortisol y los esteroides sexuales de la corteza suprarrenal se sintetizan por virtud de la acción de la hormona adrenocorticotrópica (ACTH) proveniente de la hipófisis anterior. La síntesis de aldosterona, en cambio, ocurre mayormente de manera independiente de la ACTH y se regula por el estímulo del eje renina-angiotensina. Así, frente a una insuficiencia suprarrenal primaria por daño directo de la corteza suprarrenal se presentan manifestaciones clínicas relacionadas tanto con la deficiencia de glucocorticoides como de mineralocorticoides, mientras que en el caso de insuficiencia suprarrenal secundaria (debida a daño hipofisiario) no se suelen presentar manifestaciones relacionadas con déficit salino (figura 5). La insuficiencia suprarrenal primaria ocasionada por el daño directo de las glándulas suprarrenales corresponde a lo que genéricamente se ha conocido como “enfermedad de Addison”. La insuficiencia suprarrenal secundaria es, con mucha frecuencia, el resultado de la suspensión de la administración de glucocorticoides exógenos. Los esteroides, al inhibir la producción
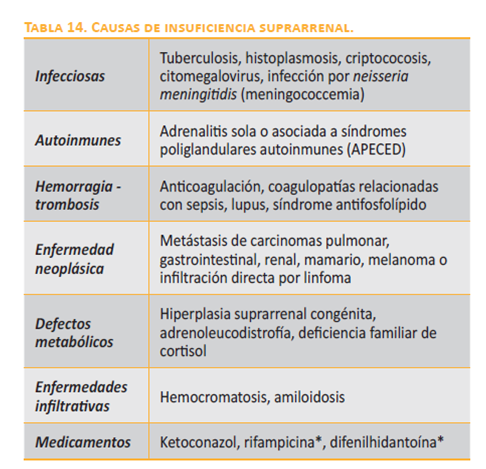
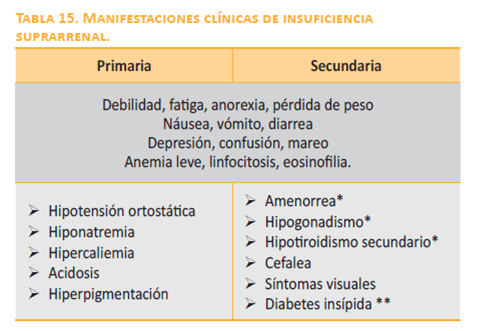
endógena de corticotropina pueden conducir a atrofia suprarrenal que puede prolongarse hasta varias semanas después de suspendida su administración exógena. En la mayoría de los casos, esta atrofia no involucra la zona glomerulosa de la corteza suprarrenal, la cual mantiene intacta su producción de aldosterona que depende del estímulo del eje renina-angiotensina. Las causas más comunes de insuficiencia suprarrenal se listan en la tabla 14. Otras causas de insuficiencia suprarrenal secundaria incluyen tumores de la glándula hipófisis o de la base del cráneo, enfermedades granulomatosas como sarcoidosis o histiocitosis X que afectan el tejido hipofisiario, síndrome de Sheehan o hemorragia hipofisiaria, trauma de la base del cráneo o cirugía hipofisiaria. En el contexto ambulatorio, el déficit de cortisol se asocia con anorexia, debilidad, náusea, pérdida de peso y síntomas relacionados con hipoglucemia o neuroglucopenia. El déficit de aldosterona, por otra parte, puede conducir a deshidratación grave, mayor hipotensión y acidosis (tabla 15). |
Insuficiencia suprarrenal en el paciente crítico:
En circunstancias clínicas como infección grave, trauma severo, quemaduras, o en casos de cirugía mayor, el incremento en las necesidades metabólicas puede llevar a elevación de los niveles de cortisol plasmático, los cuales pueden alcanzar hasta seis veces el nivel habitual. En sujetos que no posean una “reserva funcional” suficiente, la enfermedad crítica puede precipitar ICREC, cuyas manifestaciones clínicas no serán tan evidentes. En este contexto, la sospecha de insuficiencia suprarrenal se suscita por la presencia de inestabilidad hemodinámica aun con un adecuado aporte de líquidos, o bien ante la evidencia de estado inflamatorio persistente sin un foco definido y que no responde al tratamiento establecido. Así, es posible que en los enfermos críticos no sea posible reconocer un daño estructural adrenal o hipofisiario, aunque sí exista una insuficiencia funcional clínicamente apreciable. El eje hipotálamo-hipófisis-suprarrenal se activa durante las fases agudas de la enfermedad, aumentando la liberación de cortisol, incrementando el porcentaje de cortisol libre con relación al total y favoreciendo la translocación del complejo GC receptor hacia el núcleo. En los últimos años se ha acuñado el término ICREC(83) (insuficiencia corticosteroidea relacionada con la enfermedad crítica) que se define como la actividad corticosteroidea celular insuficiente o inadecuada para la severidad de la enfermedad del paciente. Estos cambios se han descrito en situaciones como SDRA y sepsis, pero hipotéticamente se podría esperar una respuesta similar en cualquier estado de enfermedad crítica, Diagnóstico: En el contexto de urgencias o del cuidado intensivo, el diagnóstico está basado en los hallazgos clínicos y en unos pocos paraclínicos. Así, la presencia de hipotensión asociada a hiponatremia, hipercaliemia, acidosis y excreción urinaria de sodio normal o elevada, deben hacer sospechar insuficiencia suprarrenal primaria. Manifestaciones similares, sin hipercaliemia ni acidosis, pero asociadas a rasgos de hipopituitarismo como hipotiroidismo, hipogonadismo, o diabetes insípida, suscitan la sospecha de insuficiencia suprarrenal secundaria. A las manifestaciones anteriores pueden sumarse dolor abdominal, fiebre, linfocitosis o eosinofilia. Para confirmar la insuficiencia suprarrenal se han usado diversas pruebas entre las cuales se cuentan la determinación de cortisol plasmático (urinario o en saliva), la determinación de 17– hidroxiesteroides urinarios, la medición directa de ACTH, las pruebas de estímulo con ACTH o las pruebas de hipoglucemia inducida por infusión de insulina. En condiciones normales, el cortisol presenta variaciones circadianas que dificultan su interpretación; así, en la mañana los valores normales oscilan entre 3 y 20 mg/mL, mientras que en la noche pueden encontrarse por debajo de 3 mg/mL. Se debe tener en cuenta que la insuficiencia suprarrenal puede establecerse en el curso de varios días en el paciente inestable, de manera que haber descartado su presencia en un momento dado, no significa que no pueda presentarse luego en el curso de la enfermedad. Tratamiento: La restitución de sodio y líquidos, así como el uso de soluciones dextrosadas cuando haya hipoglucemia asociada, constituyen la base del tratamiento. Cuando se establece el diagnóstico de ICREC, el manejo involucra la administración de glucocorticoides. En las fases iniciales del tratamiento no se recomienda el uso de mineralocorticoides como fludrocortisona puesto que las dosis elevadas de glucocorticoides ejercen un buen efecto retenedor de sal. Hidrocortisona. La dosis de hidrocortisona en pacientes con choque séptico debe ser de 200 mg/día divididos en cuatro dosis (50 mg cada seis horas) o como bolo de 100 mg, seguidos de una infusión continua de 4 mg/h. El tratamiento debe retirarse de manera gradual y no abruptamente, disminuyendo gradualmente cada dos a tres días, evaluando la respuesta clínica del paciente. No se recomienda tratar a los pacientes con choque séptico e ICREC con dosis altas de hidrocortisona. |